Des de les primeres observacions que alguns supervivents de la pesta no es tornaven a posar malalts fins a les teràpies que avui modulen i reactiven les nostres defenses contra el càncer, la immunologia ha transformat profundament la medicina. El que va començar com a intuïcions sobre epidèmies i vacunes és ara una ciència clau per entendre infeccions, tumors i autoimmunitat, i per aprendre a modular les nostres defenses al llarg de la vida. Com va començar tot i què sabem avui del sistema immunològic?
Durant gran part de la història, la humanitat va combatre les malalties sense entendre-les. Les primeres idees que van donar forma a la immunologia no van sorgir de laboratoris ni de teories complexes, sinó de l’observació directa de pacients. Una de les més decisives va ser comprovar que els que sobrevivien a una epidèmia concreta rarament tornaven a contreure la mateixa malaltia.
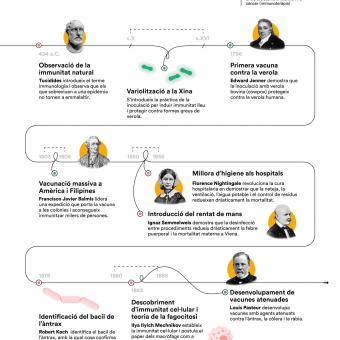
L’any 434 aC, durant la pesta d’Atenes, l’historiador Tucídides va descriure que els supervivents quedaven protegits davant de nous contagis de la malaltia, i va deixar així constància escrita d’un fenomen que avui identifiquem com a immunitat adquirida. A partir d’aquí va néixer una intuïció molt poderosa: el cos recorda les malalties i aprèn a atacar-les per defensar-se de manera més eficient en el futur.
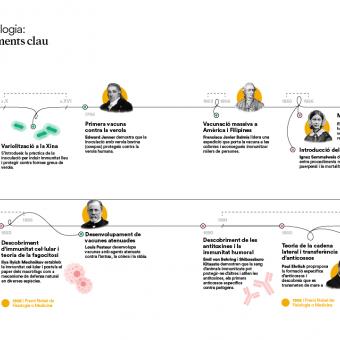
Aquesta intuïció va empènyer a buscar maneres d’infectar de manera controlada persones sanes per estimular que el seu cos fes aquest aprenentatge sense assumir totes les conseqüències de la malaltia. La pregunta no era encara què ens feia posar malalts, sinó com podíem aconseguir protecció sense morir en l’intent. Hi ha evidències que, ja al segle VI aC, a la Xina i a l’Índia es practicava la inoculació o aspiració via nasal de pols de crostes de malalts com a prevenció de la verola. Més tard, es va desenvolupar la variolització, pràctica que consistia a induir infeccions lleus de verola per evitar les formes mortals inoculant persones sanes amb material com ara pus o crostes de malalts lleus per provocar una forma atenuada de la malaltia i generar d’aquesta manera immunitat.
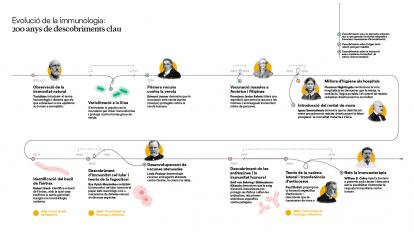
La vacuna: una revolució de la salut pública
La cerca intuïtiva de protecció mitjançant una exposició controlada al patogen es va repetir en una de les grans fites de la medicina.
La verola era una malaltia altament prevalent que causava un greu problema de salut pública. Estava distribuïda pràcticament arreu del món, no distingia edats ni classes socials i, a més, causava una mortalitat molt alta (del 30 al 60% en els no vacunats).
El 1796, el científic anglès Edward Jenner va inaugurar la vacunació moderna en demostrar amb evidència pràctica que la verola de les vaques protegia contra la verola humana. Aquest descobriment, el primer documentat científicament, es va basar en diverses experiències prèvies d’inoculacions dutes a terme per Lady Mary Wortley Montagu a Anglaterra i posteriorment per Benjamin Jesty amb verola bovina, i en la seva pròpia observació rural: les munyidores que contreien la verola vacuna no desenvolupaven la malaltia humana.
Així es va desenvolupar un dels avenços més grans en salut pública de la història, encara sense comprendre l’existència de microorganismes, cèl·lules o defenses internes. La immunologia va començar com una disciplina cega, guiada per l’evidència i els resultats, i no pel coneixement dels mecanismes implicats. La vacuna funcionava, tot i que ningú no sabia per què. L’impacte d’aquest descobriment va ser enorme i immediat.
Gairebé cent anys després dels experiments de Jenner, el químic Louis Pasteur va començar a treballar en l’àmbit de les vacunes. L’èxit de les vacunacions de Pasteur amb virus atenuats el va convertir en un heroi nacional i va facilitar la creació de diferents instituts vacunals. Avui, l’Institut Pasteur és un centre de referència en recerca biomèdica i disposa d’una xarxa de 30 instituts Pasteur distribuïts per 27 països dels 5 continents.
Higiene, infecció i sentit comú científic
Mentre el desenvolupament de les vacunes avançava per protegir contra altres malalties, una altra revolució silenciosa s’obria pas.
A la dècada del 1850 la infermera anglesa Florence Nightingale va observar que la neteja, la ventilació i l’ordre reduïen dràsticament la mortalitat hospitalària. Se’n desconeixia la causa, però aquesta pràctica salvava vides.
A mitjan segle XIX, la millora de la higiene hospitalària i la introducció del rentat de mans van reduir les morts de manera significativa. Novament, la medicina es trobava davant d’una revolució que tenia lloc sense entendre el mecanisme que hi havia darrere. No va ser fins al 1876 que el metge i microbiòleg alemany Robert Koch va identificar el bacil de l’àntrax i va demostrar definitivament que els microorganismes causaven malalties. De cop, tot encaixava: la higiene no era només important per mantenir l’ordre, sinó que era sobretot una poderosa barrera contra enemics invisibles. Per primera vegada es descrivia el concepte de patogen com a enemic que atacava el nostre cos, però encara faltava comprendre qui era el seu defensor.
Un exercit invisible dins del cos
Les grans preguntes de la medicina llavors van canviar de direcció. Ja no es tractava només d’identificar què ens emmalaltia, sinó de descobrir quines armes tenia el cos per defensar-se, on eren i com funcionaven.
El desenvolupament de noves tecnologies com el microscopi i la posada a punt de tècniques de cultiu cel·lular van permetre descobrir que l’organisme està poblat de cèl·lules especialitzades. A finals del segle XIX, el microbiòleg Ilià Ilitx Métxnikov va descobrir que algunes d’aquestes cèl·lules eren capaces d’engolir patògens, processos que va batejar com a fagocitosi. Altres cèl·lules especialitzades eren capaces de reconèixer cèl·lules infectades i d’eliminar-les o fins i tot de produir substàncies que neutralitzaven la infecció d’altres cèl·lules.
A poc a poc es va anar descrivint i comprenent el que ara coneixem com a sistema immunitari: el conjunt de cèl·lules, teixits i òrgans que protegeixen el cos de substàncies estranyes i cèl·lules danyoses. El sistema immunitari comprèn, per tant, una multiplicitat de tipus cel·lulars, com els limfòcits T i B, els neutròfils, les cèl·lules dendrítiques, etc.: òrgans com la medul·la òssia, el tim i la melsa, i també molècules com els anticossos.
Una característica clau d’aquest sistema és la seva capacitat d’anticipació; l’organisme ja disposa d’un ampli repertori de limfòcits amb receptors diferents que són capaços de reconèixer diferents elements estranys. Quan aquests apareixen, els limfòcits que els reconeixen són capaços de produir anticossos específics contra ells. El sistema immunitari actua com si tingués moltes claus i estigués preparat per obrir infinitat de panys.
Memòria: el veritable aprenentatge immunològic
Quan un dels limfòcits d’aquest exèrcit preparat troba el seu pany s’activa la resposta immunològica contra allò que cal destruir: el limfòcit que s’activa es comença a multiplicar (es diu que es clona) per crear un gran nombre de soldats especialitzats. Aquest nou exèrcit especialitzat es divideix entre els que participen en l’eliminació dels elements estranys i els que produeixen anticossos per bloquejar aquests elements.
Quan acaba la batalla, no tot desapareix. Queden unes poques cèl·lules de memòria, entrenades i llestes per respondre més de pressa si «l’enemic» torna. Aquestes són les cèl·lules que els científics volen generar amb cada vacuna. A més, en alguns casos queden cèl·lules plasmàtiques de llarga vida capaces de continuar produint anticossos durant anys. Induir aquest tipus de protecció duradora també és un dels objectius de les vacunes.
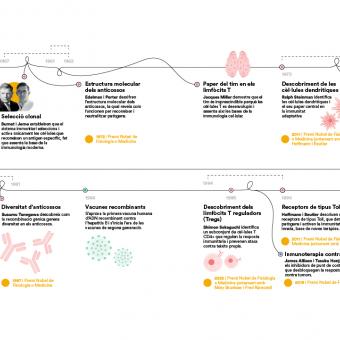
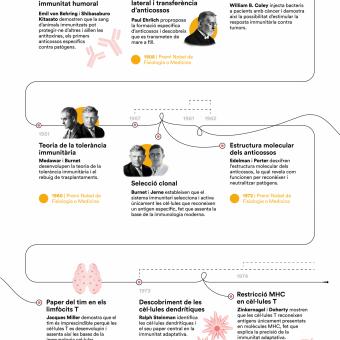
Aquest principi, establert durant el segle XX amb teories com la selecció clonal, iniciada amb els estudis de Frank Macfarlane Burnet i la teorització de Niels Kaj Jerne, tots dos immunòlegs, explica per què una infecció o una vacunació poden protegir durant anys i fins i tot dècades.
Quan l’enemic és dins
El sistema immunològic no tracta només infeccions externes. El cos està també preparat per defensar-nos de l’aparició de cèl·lules malignes. Aquesta idea, avui central en oncologia, té un origen sorprenent.
A finals del segle XIX, el metge nord-americà Willian B. Coley va observar que un pacient amb un tumor millorava després d’una infecció local. Així va néixer la immunoteràpia, de nou a partir d’una evidència de la qual es desconeixien els mecanismes. Avui sabem que darrere d’aquesta sorprenent observació hi havia el sistema immunitari, amb limfòcits que ataquen específicament cèl·lules tumorals.
El problema és que el càncer juga amb avantatge respecte de les cèl·lules dels patògens. Les cèl·lules tumorals són pròpies i, per això, moltes vegades passen desapercebudes. «El sistema immunitari ha hagut d’evolucionar per ser molt precís en allò que fa, atacant les infeccions com els virus o els bacteris, però tolerant els teixits normals. Per aquest motiu, el sistema immunitari ha desenvolupat un seguit de controls per activar-se o inactivar-se segons cal. El càncer de tot això n’ha après, i intenta amagar-se utilitzant els controls negatius del sistema immune», explica Antoni Ribas, president del Consell Assessor Científic del CaixaResearch Institute.
El descobriment dels inhibidors de punts de control immunitaris (checkpoint inhibitors) a finals del segle XX per part dels immunòlegs James Allison i Tasuku Honjo va permetre desbloquejar aquesta resposta i va demostrar que es pot reactivar el sistema immunològic per combatre tumors avançats. Va ser una revolució en la immunoteràpia del càncer que els va fer mereixedors del Nobel de Medicina el 2019.
El delicat equilibri entre defensa i tolerància
Aquest mateix sistema de control explica altres fenòmens. La capacitat del sistema immunitari de distingir entre el que és propi i el que és aliè al nostre cos és al darrere, per exemple, del rebuig als òrgans trasplantats. A més, quan la tolerància al que és propi falla, es poden desenvolupar les conegudes com a malalties autoimmunes.
«En un moment determinat, el sistema immunitari pot funcionar de manera inapropiada. Això es pot manifestar com una resposta exagerada davant d’antígens innocus, cosa que passa en les malalties al·lèrgiques, o com una pèrdua de tolerància als antígens propis, que dona lloc a malalties autoimmunes», explica Josep Tabernero, president del Comitè Científic del CaixaResearch Institute.
L’autoimmunitat no és una sola malaltia, sinó un conjunt de desordres. Pot afectar diferents òrgans, presenta uns desencadenants que combinen genètica i ambient, i poden convertir una resposta transitòria en un problema crònic.
«Les respostes autoimmunes inclouen múltiples patologies, com l’esclerosi múltiple quan el sistema immunològic danya determinats components del cervell, la diabetis quan danya el pàncrees, l’artritis reumatoide quan danya components articulars o la psoriasi en el cas de la pell», assenyala Gabriel Rabinovich, investigador principal al CaixaResearch Institute.
Comprendre com es manté la tolerància i per què a vegades es perd és un dels grans reptes actuals de la immunologia.
Precisió: el nou llenguatge de la immunologia
Avui es coneixen força bé les regles del joc de la immunologia, però no prou encara. Sabem que hi ha pacients que responen a una teràpia i després deixen de fer-ho. Resoldre aquesta incògnita és clau per al futur de la medicina.
«Gran part de la investigació justament se centra a comprendre per què passa això: per què alguns reaccionen favorablement i d’altres no, si els mecanismes són generals i específics de cada patologia i de cada persona. La medicina de precisió busca precisament entendre aquests mecanismes individuals i característics per abordar-los de manera personalitzada en diferents grups o de manera individual», recalca el doctor Rabinovich.
«Cada vegada hi ha més evidència de la importància de l’estat basal immunològic, ja que aquest pot predir i determinar com respondrem a les vacunes o a les infeccions i altres malalties», explica Gemma Moncunill, investigadora principal al CaixaResearch Institute. L’estat basal descriu la configuració i el funcionament del sistema immunitari d’un individu en condicions normals. Aquests estat depèn de factors genètics, però també de factors ambientals com la contaminació, l’estil de vida o les infeccions prèvies de la persona.
Mirar la salut amb una nova lent
Avui s’entenen millor les fronteres del cos, els microorganismes i les defenses, però queda marge per afinar, personalitzar i maximitzar el benefici terapèutic. Les preguntes actuals ja no es limiten a determinar com defensar-nos, sinó que també es plantegen com podem modular, entrenar i acompanyar el sistema immunològic al llarg de la vida. Per aquest motiu, el CaixaResearch Institute té com a objectiu situar la immunologia al centre de la salut, no tan sols com una ambició científica, sinó també com una necessitat per respondre als grans reptes mèdics del present i del futur.