Desde las primeras observaciones de que algunos supervivientes de la peste no volvían a padecerla hasta las terapias que hoy modulan y reactivan nuestras defensas contra el cáncer, la inmunología ha transformado por completo la medicina. Lo que surgió como intuiciones sobre epidemias y vacunas es ahora una ciencia clave para entender infecciones, tumores y autoinmunidad, y para aprender a modular nuestras defensas a lo largo de la vida. ¿Cómo empezó todo y qué sabemos hoy del sistema inmunológico?
Durante la mayor parte de la historia, la humanidad combatió las enfermedades sin entenderlas. Las primeras ideas que dieron forma a la inmunología no surgieron de laboratorios ni de teorías complejas, sino de la observación directa de pacientes. Una de las más decisivas fue comprobar que quienes sobrevivían a una epidemia concreta rara vez volvían a padecer la misma enfermedad.
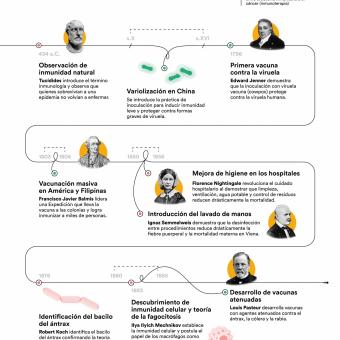
En el año 434 a. C., durante la peste de Atenas, el historiador Tucídides describió que los supervivientes quedaban protegidos frente a nuevos contagios de la enfermedad, dejando así constancia escrita de un fenómeno que hoy identificamos como inmunidad adquirida. A partir de ahí nació una intuición poderosa: el cuerpo recuerda las enfermedades y aprende a atacarlas para defenderse de manera más eficiente en el futuro.
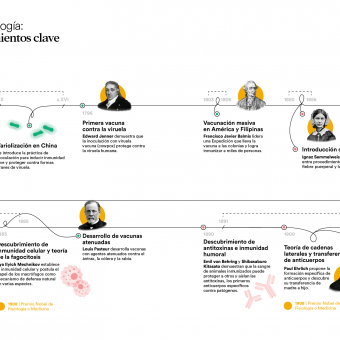
Esa intuición empujó a buscar maneras de infectar de modo controlado a personas sanas para estimular ese aprendizaje en su cuerpo sin asumir todas las consecuencias de la enfermedad. La pregunta no era aún qué nos enferma, sino cómo lograr protección sin morir en el intento. Existen evidencias de que ya en el siglo VI a. C., en China y en India se practicaba la inoculación o aspiración vía nasal de polvo de costras de enfermos como prevención de la viruela. Más tarde se desarrolló la variolización, una práctica que consistía en inducir infecciones leves de viruela para evitar las formas mortales inoculando a personas sanas con material como pus o costras de enfermos leves para provocar una forma atenuada de la enfermedad y así generar inmunidad.
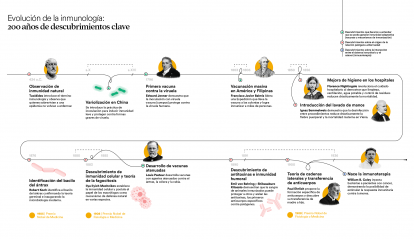
La vacuna: una revolución de la salud pública
La búsqueda intuitiva de protección mediante una exposición controlada al patógeno se repitió en uno de los grandes hitos de la medicina.
La viruela era una enfermedad altamente prevalente que causaba un grave problema de salud pública. Estaba distribuida por casi todo el mundo, no distinguía edades ni clases sociales y además causaba alta mortalidad (del 30 al 60 % en los no vacunados).
En 1796, el científico inglés Edward Jenner inauguró la vacunación moderna al demostrar con evidencia práctica que la viruela de las vacas protegía frente a la viruela humana. Su descubrimiento, el primero documentado científicamente, se basó en diversas experiencias previas de inoculaciones realizadas por Lady Mary Wortley Montagu en Inglaterra y posteriormente por Benjamin Jesty con viruela bovina, y en su propia observación rural: las ordeñadoras que contraían viruela vacuna no desarrollaban la enfermedad humana.
Así se desarrolló uno de los mayores avances en salud pública de la historia, aun sin comprender la existencia de microorganismos, células o defensas internas. La inmunología empezó como una disciplina ciega, guiada por la evidencia y los resultados, no por el conocimiento de los mecanismos implicados. La vacuna funcionaba, aunque nadie sabía por qué. El impacto de este descubrimiento fue enorme e inmediato.
Casi cien años después de los experimentos de Jenner, el químico Louis Pasteur inició sus trabajos en vacunas. El éxito de las vacunaciones de Pasteur con virus atenuados lo convirtió en un héroe nacional y facilitó la creación de distintos institutos vacunales. Hoy, el Instituto Pasteur es un centro de referencia en investigación biomédica y cuenta con una red de 30 institutos Pasteur distribuidos por 27 países de los 5 continentes.
Higiene, infección y sentido común científico
Mientras el desarrollo de las vacunas avanzaba para proteger contra otras enfermedades, otra revolución silenciosa se abría paso.
En la década de 1850 la enfermera inglesa Florence Nightingale observó que la limpieza, la ventilación y el orden reducían drásticamente la mortalidad hospitalaria. Se desconocía la causa, pero la práctica salvaba vidas.
A mediados del siglo XIX, la mejora de la higiene hospitalaria y la introducción del lavado de manos redujeron las muertes de forma significativa. De nuevo, la medicina se encontraba frente a una revolución que tenía lugar sin entender el mecanismo que había detrás. No fue hasta 1876 cuando el médico y microbiólogo alemán Robert Koch identificó el bacilo del ántrax y demostró definitivamente que los microorganismos causaban enfermedades. De pronto, todo encajaba: la higiene no era solamente importante para mantener el orden, sino que era sobre todo una poderosa barrera contra enemigos invisibles. Por primera vez se describía el concepto de patógeno como enemigo atacante de nuestro cuerpo, pero aún faltaba comprender quién era su defensor.
Un ejército invisible dentro del cuerpo
Las grandes preguntas de la medicina cambiaron entonces de dirección. Ya no se trataba solamente de identificar qué nos enfermaba, sino de descubrir qué armas tenía el cuerpo para defenderse, dónde estaban y cómo funcionaban.
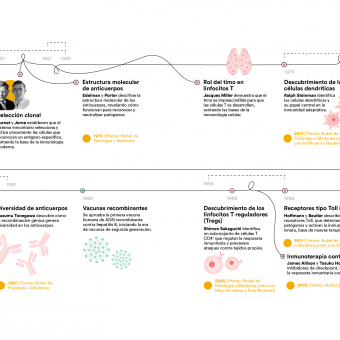
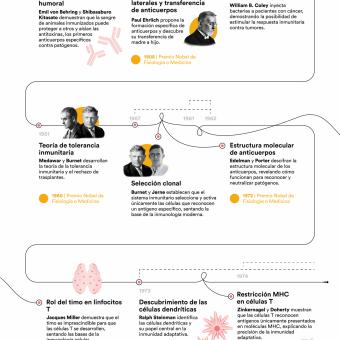
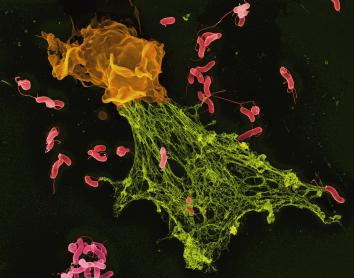
El desarrollo de nuevas tecnologías como el microscopio electrónico y la puesta a punto de técnicas de cultivo celular permitieron descubrir que el organismo está poblado por células especializadas. A finales del siglo XIX, el microbiólogo Ilya Ilyich Mechnikov descubrió que algunas de estas células eran capaces de engullir patógenos, proceso que bautizó como fagocitosis. Otras células especializadas eran capaces de reconocer células infectadas y eliminarlas o incluso de producir sustancias que neutralizaban la infección de otras células.
Poco a poco se fue describiendo y comprendiendo lo que ahora conocemos como sistema inmunitario: el conjunto de células, tejidos y órganos que protegen el cuerpo de sustancias extrañas y células dañinas. El sistema inmunitario comprende por tanto una multiplicidad de tipos celulares, como los linfocitos T y B, los neutrófilos, las células dendríticas, etc.; órganos como la médula ósea, el timo y el bazo, y también moléculas como los anticuerpos.
Una característica clave de este sistema es su capacidad de anticipación; el organismo ya dispone de un amplio repertorio de linfocitos con receptores distintos que son capaces de reconocer diferentes elementos extraños. Cuando estos aparecen, los linfocitos que los reconocen son capaces de producir anticuerpos específicos contra ellos. El sistema inmunitario actúa como si tuviera muchas llaves y estuviera preparado para abrir infinidad de cerraduras.
Memoria: el verdadero aprendizaje inmunológico
Cuando uno de los linfocitos de este ejército preparado encuentra su cerradura se activa la respuesta inmunológica contra aquello que hay que destruir: el linfocito que se activa comienza a multiplicarse (se dice que se clona) para crear un gran número de soldados especializados. Este nuevo ejército especializado se divide entre los que participan en la eliminación de los elementos extraños y los que producen anticuerpos para bloquear esos elementos.
Cuando la batalla termina, no todo desaparece. Permanecen unas pocas células de memoria, entrenadas y listas para responder con mayor rapidez si «el enemigo» regresa. Estas son las células que los científicos pretenden generar con cada vacuna. Además, en algunos casos permanecen células plasmáticas de larga vida capaces de seguir produciendo anticuerpos durante años. Inducir este tipo de protección duradera también es uno de los objetivos de las vacunas.
Este principio, establecido durante el siglo XX con teorías como la selección clonal, iniciada con los estudios de Frank Macfarlane Burnet y la teorización de Niels Kaj Jerne, ambos inmunólogos, explica por qué una infección o una vacunación pueden proteger durante años e incluso décadas.
Cuando el enemigo está dentro
El sistema inmunológico no trata únicamente infecciones externas. El cuerpo está también preparado para defendernos de la aparición de células malignas. Esta idea, hoy central en oncología, tiene un origen sorprendente.
A finales del siglo XIX, el médico norteamericano Willian B. Coley observó que un paciente con un tumor mejoraba tras una infección local. Así nació la inmunoterapia, de nuevo a partir de una evidencia de la que se desconocían los mecanismos. Hoy sabemos que detrás de esa sorprendente observación estaba el sistema inmunitario, con linfocitos atacando específicamente células tumorales.
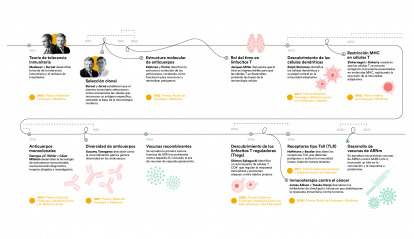
El problema es que el cáncer juega con ventaja con respecto a las células de los patógenos. Las células tumorales son propias y, por ello, muchas veces pasan desapercibidas. «El sistema inmunitario ha tenido que evolucionar para ser muy preciso en lo que hace, atacando las infecciones como los virus o las bacterias, pero tolerando los tejidos normales. Por ese motivo, el sistema inmunitario ha desarrollado una serie de controles para activarse o inactivarse según se necesita. El cáncer ha aprendido de esto e intenta esconderse usando los controles negativos del sistema inmune», explica Antoni Ribas, presidente del Consejo Asesor Científico del CaixaResearch Institute.
El descubrimiento de los inhibidores de puntos de control inmunitarios (checkpoint inhibitors) a finales del siglo XX por parte de los inmunólogos James Allison y Tasuku Honjo permitió desbloquear esa respuesta y demostró que el sistema inmunológico puede ser reactivado para combatir tumores avanzados. Fue una revolución en la inmunoterapia del cáncer que les valió el Nobel de Medicina en 2019.
El delicado equilibrio entre defensa y tolerancia
Ese mismo sistema de control explica otros fenómenos. La capacidad del sistema inmunitario de distinguir entre lo propio y lo ajeno a nuestro cuerpo está detrás, por ejemplo, del rechazo a los órganos trasplantados. Además, cuando la tolerancia a lo propio falla, se pueden desarrollar las conocidas como enfermedades autoinmunes.
«En un momento determinado, el sistema inmunitario puede funcionar de manera inapropiada. Esto puede manifestarse como una respuesta exagerada frente a antígenos inocuos, lo que ocurre en las enfermedades alérgicas, o como una pérdida de tolerancia a los antígenos propios, que da lugar a enfermedades autoinmunes», explica Josep Tabernero, presidente del Comité Científico del CaixaResearch Institute.
La autoinmunidad no es una sola enfermedad, sino un conjunto de desórdenes. Puede afectar a distintos órganos, sus desencadenantes combinan genética y ambiente, y pueden convertir una respuesta transitoria en un problema crónico.
«Las respuestas autoinmunes incluyen múltiples patologías, como la esclerosis múltiple cuando el sistema inmunológico daña determinados componentes del cerebro, la diabetes cuando daña el páncreas, la artritis reumatoide cuando daña componentes articulares o la psoriasis en el caso de la piel», señala Gabriel Rabinovich, investigador principal en el CaixaResearch Institute.
Comprender cómo se mantiene la tolerancia y por qué a veces se pierde es uno de los grandes retos actuales de la inmunología.
Precisión: el nuevo lenguaje de la inmunología
Hoy se conocen bastante bien las reglas del juego de la inmunología, pero no lo suficiente. Sabemos que hay pacientes que responden a una terapia y luego dejan de hacerlo. Resolver esta incógnita es clave para el futuro de la medicina.
«Gran parte de la investigación se centra justamente en comprender por qué sucede eso: por qué algunos reaccionan favorablemente y otros no, si los mecanismos son generales o específicos de cada patología y de cada persona. La medicina de precisión busca precisamente entender esos mecanismos individuales y característicos para abordarlos de manera personalizada en distintos grupos o de manera individual», recalca el doctor Rabinovich.
«Cada vez hay más evidencia de la importancia del estado basal inmunológico, ya que este puede predecir y determinar cómo responderemos a las vacunas o a las infecciones y otras enfermedades», explica Gemma Moncunill, investigadora principal en el CaixaResearch Institute. El estado basal describe la configuración y el funcionamiento del sistema inmunitario de un individuo en condiciones normales. Ese estado depende de factores genéticos, pero también de factores ambientales como la contaminación, el estilo de vida o las infecciones previas de la persona.
Mirar la salud con una nueva lente
Hoy se entienden mejor las fronteras del cuerpo, los microorganismos y las defensas, pero queda margen para afinar, personalizar y maximizar el beneficio terapéutico. Las preguntas actuales ya no se limitan a cómo defendernos, sino que también se plantean cómo modular, entrenar y acompañar al sistema inmunológico a lo largo de la vida. Por ese motivo, el CaixaResearch Institute tiene como objetivo poner la inmunología en el centro de la salud, no solo como una ambición científica, sino también como una necesidad para responder a los grandes desafíos médicos del presente y del futuro.