
Estás leyendo:

Estás leyendo:

16.05.24
10 minutos de lecturaEnvía tus preguntas a:
Científico titular del CSIC y director del grupo de Biología Molecular de las Infecciones
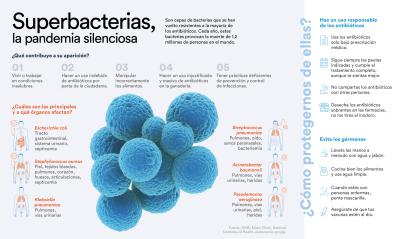
Cada año en el mundo 1,2 millones de personas mueren por infecciones causadas por bacterias resistentes a los antibióticos. Según la OMS, la capacidad de las bacterias para adaptarse y resistir a los fármacos diseñados para combatirlas es ya una de las mayores amenazas para la salud pública mundial. Si no se frena su aumento, la resistencia antimicrobiana podría provocar hasta 10 millones de muertes en el mundo en 2050. En cuatro proyectos de investigación subvencionados por las convocatorias CaixaResearch de Investigación en Salud y CaixaImpulse de Innovación en Salud de 2023 se busca hacer frente a este gran reto para la humanidad con abordajes muy distintos.
Cuando Daniel López Serrano, bioquímico del Centro Nacional de Biotecnología del Consejo Superior de Investigaciones Científicas, empezó a hacer ciencia básica en un laboratorio a principios de los años 2000 y solicitaba muestras a los hospitales, se encontraba con una sola superbacteria entre las 20 muestras que recibía. Hoy en día, lo normal es que las 20 muestras contengan bacterias resistentes a los antibióticos. Por eso, descubrir un nuevo antibiótico eficaz es un gran desafío para la industria farmacéutica. «La investigación puede durar décadas sin garantías de que se obtengan resultados y la farmacorresistencia aparece cada vez más rápido, cosa que desincentiva la inversión en investigación y desarrollo de nuevos antimicrobianos», explica López Serrano.

El proyecto que lidera este investigador tiene por objetivo recuperar la eficacia de los antibióticos que han dejado de funcionar por el aumento de bacterias resistentes. Su equipo descubrió en 2010 un proceso celular esencial para la supervivencia de las bacterias durante las infecciones. Lo explica así: «Este mecanismo se encarga de estabilizar y ensamblar las maquinarias proteicas que tiene la bacteria, incluidas las maquinarias responsables de la resistencia a los antibióticos. Estos años nos hemos dedicado a entender este mecanismo y hemos podido diseñar tratamientos que lo inhiben. Con ello conseguimos que todas esas maquinarias no se puedan ensamblar». En esta situación, la administración de los antibióticos clásicos funciona porque las bacterias tienen los mecanismos de resistencia desactivados.
Según López Serrano, la gran ventaja de este proyecto, que ha recibido una subvención de 494.300 euros de la convocatoria CaixaResearch de Investigación en Salud 2023, es precisamente que se propone un tratamiento capaz de curar infecciones que no se podrían curar y lo hace mediante la reactivación de antibióticos comercialmente disponibles.
«Lo que hemos descubierto no es una molécula, es un mecanismo, por lo que lo más directo para implementarlo seguramente será desarrollarlo como proceso o terapia hospitalaria, más que comercializarlo», argumenta el investigador. «Hasta ahora hemos diseñado el procedimiento para un par de especies bacterianas y vamos a intentar expandir ese conocimiento a otras especies, las más frecuentes en los hospitales, para crear un tratamiento que sea universal».
Cuando se desarrolla un nuevo antibiótico puede suceder que, aunque tenga capacidad para atacar la bacteria, no consiga atravesar su membrana. Las estrategias actuales para facilitar ese traspaso de la membrana no han conseguido ser totalmente eficaces. El proyecto que lidera Javier Montenegro, químico del Centro Singular de Investigación en Química Biológica y Materiales Moleculares (CiQUS) de la Universidade de Santiago de Compostela, en colaboración con Mariana Pinho, de la Universidade Nova de Lisboa, utiliza una nueva aproximación para transportar los antibióticos al interior de las bacterias que tiene mucho potencial para habilitar el uso de antibióticos ya existentes en cepas resistentes o de permeabilidad limitada.

«Se trata de un reto muy complejo, pues no resulta fácil atravesar la membrana de las bacterias, sobre todo las de las bacterias llamadas gramnegativas, que tienen una membrana externa que supone una barrera adicional», explica Montenegro. En muchas ocasiones, las aproximaciones actuales «usan lípidos para atravesar membranas formadas por otros lípidos», lo que requiere «la encapsulación de las moléculas y eso puede afectar tanto a su estabilidad como a la liberación del antibiótico en el momento adecuado», añade.
Sin embargo, el equipo de Montenegro y Pinho ha descubierto una propiedad de los clústeres de boro que permite el paso de moléculas hidrófilas —moléculas que se disuelven en el agua— a través de membranas lipídicas. Para Montenegro, este gran hito científico, que ha recibido 984.050 euros de la convocatoria CaixaResearch de Investigación en Salud 2023, supone «un cambio completo de paradigma para la ciencia y la entrega de fármacos. Es una investigación muy novedosa y completamente diferente al dogma establecido. Ahora necesitamos entender cuáles son las bases de este mecanismo para poder aplicarlas al transporte de antibióticos».
Aunque los antibióticos pueden eliminar microorganismos, paradójicamente también contribuyen a la aparición de bacterias resistentes y facilitan su proliferación en un entorno libre de competidores. Asimismo, hoy en día el desarrollo de antibióticos sufre un estancamiento.
Por este motivo, algunos proyectos de investigación se están centrando en desarrollar estrategias terapéuticas alternativas para desactivar la virulencia de las superbacterias y resensibilizarlas a los antibióticos, preservando al mismo tiempo la microbiota, la comunidad bacteriana natural de nuestro organismo, que puede verse alterada por los tratamientos habituales con antibióticos. Este delicado ecosistema juega un rol esencial en nuestra salud intestinal, dermatológica y mental, así como en nuestro sistema inmunológico, nuestras defensas contra los patógenos, nuestro metabolismo y la regulación de nuestro peso corporal.

El equipo de Didier Cabanes, biólogo molecular del Instituto de Investigação e Inovação em Saúde de la Universidade do Porto, estudia las bacterias grampositivas, como los estafilococos, los estreptococos y Listeria. En la pared celular de Listeria descubrió que «algunos glicopolímeros (azúcares) presentes en su superficie —que no eran determinantes para su crecimiento— eran cruciales no solo para la resistencia de la bacteria a las defensas antimicrobianas del huésped y a los antibióticos, sino también para la patogenicidad bacteriana». Por este motivo, los investigadores creen que «las enzimas responsables de la presencia de estos glicopolímeros en la superficie bacteriana son prometedoras dianas para los fármacos antimicrobianos contra patógenos grampositivos».
El proyecto, en colaboración con la Fundação para a Ciência e a Tecnologia (FCT), ha recibido una subvención de 499.950 euros de la convocatoria CaixaResearch de Investigación en Salud 2023. Su objetivo final es desarrollar fármacos antimicrobianos de «nueva generación» que, al inhibir los glicopolímeros presentes en la superficie de las superbacterias, disminuyan su virulencia sin matarlas. Así, poco a poco, se harán susceptibles a las defensas del huésped y se conseguirá potenciar la acción de los antibióticos preservando la microbiota. «Nuestro enfoque es el primero que desarmará y sensibilizará simultáneamente los patógenos grampositivos sin afectar su crecimiento», concluye Cabanes.
En el último informe de la agencia European Centre for Disease Prevention and Control, la bacteria Klebsiella pneumoniae se hallaba entre los tres principales causantes de infecciones resistentes a antibióticos. Concretamente, en 2022 se detectaron más de 45.000 casos de infección por esta bacteria en Europa, más de un 15 % de ellos, causado por cepas inmunes al efecto de estos fármacos. Esta es la razón por la que la OMS ha clasificado Klebsiella pneumoniae entre las especies de preocupación crítica en el ámbito sanitario y por la que el equipo liderado por Mireia López Siles, microbióloga de la Universitat de Girona, decidió desarrollar una vacuna para seguir luchando contra esta bacteria.
Klebsiella pneumoniae es una bacteria que se puede encontrar en cualquier ambiente. En el entorno hospitalario, suele transmitirse por contacto con la piel, mucosas, heces, heridas u orina de una persona infectada. La situación empeora cuando la cepa que causa la infección es, además, resistente a los antibióticos. Disponer de una vacuna podría aumentar la duración de la protección frente a la bacteria en comparación con el tratamiento antibiótico, proporcionar inmunidad de grupo y reducir la mortalidad asociada a estas infecciones. «Esto es clave porque permitiría reducir el uso de antibióticos para tratar infecciones y la probabilidad de que aparezcan más bacterias resistentes a estos», explica López Siles.

El proyecto, que ha recibido 50.000 euros de la convocatoria CaixaImpulse de Innovación en Salud (financiación que se complementa con el acompañamiento por parte de expertos y mentores), se halla en fase preclínica. Su objetivo en esta fase es evaluar la capacidad de protección in vivo de KlebsiGene, una vacuna de ADN desarrollada previamente por la Universitat de Girona y el Instituto de Salud Carlos III, y mejorar su formulación. Incluye dos innovaciones principales, apunta la investigadora: «Por un lado, la vacuna se dirige a partes de la bacteria que no han sido utilizadas previamente en otras vacunas y que juegan un papel fundamental en la supervivencia de la bacteria, por lo que esperamos que confiera una mejor protección. Por otro lado, utilizamos una nueva tecnología de ADN que incorpora elementos para estimular la respuesta inmune del paciente».
Hasta el momento, el equipo que lidera López Siles ha desarrollado ocho prototipos de vacuna y ha comprobado que las células humanas interpretan correctamente la información que le proporcionan esas vacunas. «También hemos visto, mediante predicción con herramientas de bioinformática, que no todos los candidatos vacunales funcionarían igual de bien para generar una respuesta inmune. Esto nos ha permitido priorizar los prototipos para realizar pruebas de eficacia con los más prometedores. Ahora acabamos de completar la fase de producción de dos de ellos. El siguiente paso es demostrar en un organismo complejo que nuestra vacuna es capaz de activar el sistema inmunitario y proteger frente a la infección».
El desarrollo de esta vacuna «mejorará la calidad de vida de las personas con riesgo de padecer una infección por este microorganismo, especialmente en el ámbito hospitalario», añade la investigadora. Y además, al tratarse de una vacuna de ADN, es fácilmente adaptable a otros patógenos, «ya que contiene un fragmento de ADN específico que codifica para el antígeno (la parte que permitirá desarrollar la respuesta inmune), que en nuestro caso es específico de Klebsiella pneumoniae. Cambiando este fragmento por otro que codifique para un antígeno de cualquier otro microorganismo, obtendríamos una vacuna dirigida a esa otra especie. Y también podría diseñarse para prevenir infecciones por varios patógenos simultáneamente, si se incluyen secuencias de antígeno para ambos».
Este aumento generalizado de las superbacterias «es, en parte, natural —las bacterias evolucionan y van adquiriendo resistencia—», explica López Serrano, «pero con nuestro uso de los antibióticos también hemos contribuido a generar entornos, como los hospitales o la ganadería (donde se han utilizado los antibióticos de forma generalizada no solo para tratar las infecciones bacterianas de los animales, sino también para promover su crecimiento, así como para prevenir enfermedades sin diagnóstico previo), que facilitan este proceso evolutivo», haciendo así que los antibióticos dejen de ser efectivos cada vez más rápido.
Hace ya tiempo que las autoridades sanitarias trabajan en estrategias para racionalizar el uso de fármacos antibióticos, entre ellas la sensibilización de la ciudadanía. Como nos recuerda Didier Cabanes, debemos usarlos «únicamente bajo prescripción médica y cuando sean realmente necesarios». Además, «los tratamientos hay que terminarlos», añade López Serrano, «y no deben almacenarse para tomarlos cuando queramos o dárselos a los vecinos. Otra cosa importante es el desecho de los antibióticos: si tiramos los antibióticos sobrantes al inodoro estos terminan vertidos al medio natural y las bacterias están ahí también, así que es muy importante depositarlos en los puntos de recogida habilitados en las farmacias». El futuro de las superbacterias está también en nuestras manos.
Para saber más sobre las superbacterias, podéis ver el debate CaixaResearch sobre este tema: