
Estás leyendo:

Estás leyendo:

03.05.24
9 minutos de lecturaEnvía tus preguntas a:
Graduada en Biotecnología y estudiante de doctorado en Ingeniería Tisular
Solicitar entrevistaKaori Mutsuda Zapater (Barcelona, 1996) es biotecnóloga. Gracias a una beca de posgrado en el extranjero de la Fundación ”la Caixa” está cursando su doctorado en Kioto, en una nueva facultad que busca soluciones para asegurar la supervivencia humana. Su especialidad son los órganos en un chip, dispositivos en miniatura con los que se crean versiones simplificadas de partes del cuerpo. Con su investigación quiere replicar uno de los procesos más importantes y desconocidos del comienzo de la vida: la implantación de un óvulo fecundado en el útero. Antes de todo esto tuvo una larga carrera en el doblaje de películas y, entre otros trabajos, puso voz a la niña de Monstruos, S.A.
Investigas en un instituto que se dedica a la supervivencia de la humanidad. ¿En qué consisten esos estudios?
Mi facultad es la más nueva de la Universidad de Kioto y en ella se ofrecen los Estudios Integrados Avanzados en Supervivencia Humana. Es un programa de cinco años que reúne a personas de diferentes ámbitos —literatura, filosofía, medicina, ingeniería, etc.— con el objetivo de que trabajen juntas para afrontar retos globales. La idea es añadir a la especialización conocimientos de liderazgo y nociones básicas de otras disciplinas: tenemos clases de otros sectores, seminarios de profesionales de la industria y estancias en el extranjero obligatorias que nos permiten incorporar esta visión global a nuestra investigación.
¿Y el objetivo principal es evitar el fin de la humanidad?
En realidad, el enfoque es bastante abierto. A esta facultad le interesa cualquier tema que tenga sentido de cara a la supervivencia humana, pero algunas personas están trabajando en el cruce de la filosofía budista con la griega, por ejemplo; otras investigan sobre geopolítica y relaciones internacionales... En mi caso, trabajo en ciencias de la salud, en el ámbito reproductivo, por lo que sí está muy relacionado con el mantenimiento de la vida.
¿Qué imagen del futuro tienen? ¿Debemos ser optimistas?
En el ámbito de la facultad, mi percepción es que esta es un área de investigación optimista y positiva; pero en lo individual hay opiniones de todo tipo. Algunas personas investigan para escenarios catastróficos, centrándose en la supervivencia básica; otras estudian las posibilidades de colonizar Marte y vivir en el espacio exterior, por ejemplo. Hay enfoques muy variados.
¿Elegiste estudiar en Japón atraída por este tema?
Me presenté dos veces al programa de becas de posgrado en el extranjero de la Fundación ”la Caixa” y, en realidad, la primera vez aposté por Cambridge, pero no me eligieron, así que decidí presentarme de nuevo al año siguiente. Finalmente decidí optar a un puesto en la Universidad de Kioto porque el grupo de investigación me interesaba mucho: no es muy común encontrar grupos que combinen disciplinas como son el cultivo celular, en concreto de células pluripotentes, y la microfluídica. La Universidad de Kioto, además, tiene muchos recursos y conocimiento en cuanto al uso de células pluripotentes (Shinya Yamanaka ganó en 2012 el Premio Nobel de Medicina por sus investigaciones en el campo de las células madre).
¿De dónde vienen tus raíces japonesas?
Mi padre es japonés, y mi madre, catalana. Él vino a estudiar a España cuando tenía unos 20 años y se quedó. Yo nací y me crié en Barcelona, y fui a la escuela catalana primero y luego al colegio japonés. Hice toda la educación obligatoria allí y después estudié en la Universidad de Barcelona. Así que en realidad he pasado toda mi vida en España.
Tras estudiar biotecnología empezaste a trabajar en una empresa farmacéutica, pero lo dejaste. ¿Por qué?
Al acabar el grado estudié un máster en Administración de Empresas (MBA, por sus siglas en inglés) que estaba enfocado a la industria farmacéutica y que incluía prácticas en una empresa. Yo siempre he querido emprender o buscar la manera de transmitir el valor científico a la sociedad, que no se quede todo en publicaciones académicas. Por eso quise ver cómo funciona el sector farmacéutico por dentro. Me gustó mucho la experiencia, pero quería explorar otros campos.
¿En qué disciplina se enmarca tu trabajo?
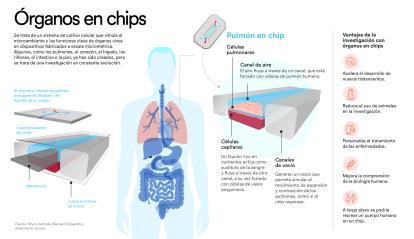
El nombre técnico es ingeniería tisular. A partir de células, en mi caso humanas, generamos tejidos y versiones simplificadas de órganos que te permiten entender cómo se desarrolla una enfermedad y cómo reacciona a distintos estímulos o fármacos, entre otras cosas. Para eso usamos una tecnología llamada «órgano en un chip», que te permite recrear órganos o partes del cuerpo (la córnea, el corazón, el cerebro, etc.) en pequeños dispositivos que se conectan unos con otros a través de unos tubitos de plástico, como si fueran venas. No es una versión en miniatura de un órgano real, sino un mecanismo que recopila sus elementos biológicos clave.
¿Juntando esos chips se podría crear un ser humano completo?
Uno de los objetivos a largo plazo es recrear el cuerpo humano en un chip. No solo un cuerpo humano, sino cada cuerpo humano, para aplicaciones de medicina personalizada. Por ahora no es del todo realista porque técnicamente es muy complejo. Además, surgen cuestiones éticas difíciles de afrontar. Una meta más asequible es simular fenómenos o enfermedades concretos. Por ejemplo, si quieres estudiar la diabetes, puedes unir un chip de un páncreas y otro de un músculo, sin la necesidad de tener representado un cuerpo humano completo.
¿Cuál es la ventaja de hacerlo a una escala tan pequeña?
Es un modelo que a la larga puede ser más económico y también más representativo. Por ejemplo, en vez de reclutar a 50 personas para un ensayo clínico, tienes miles de chips con órganos de diferentes características y obtienes datos más significativos con menos recursos. Es cierto que ahora mismo, como el proceso no está muy automatizado, requiere una mano de obra que lo encarece, pero en un futuro podría ser mucho más barato y preciso que el testado en animales.
¿El bienestar animal también es un motivo?
Mi motivación es principalmente ética, no me gusta ver sufrir a los animales. Además, la inmensa mayoría de los fármacos testados en animales no llegan al mercado porque, al probarlos con seres humanos, fallan. Solo el 2 % de esos productos se comercializa y algunos acaban retirándose por efectos adversos. Me gustaría crear un modelo alternativo que sea más barato, ético, inclusivo y representativo de lo que es el ser humano.
¿Cuál es tu proyecto de investigación concreto?
Estoy especializada en la parte reproductiva; en concreto, quiero recrear el proceso de la implantación del embrión humano usando modelos artificiales del útero y el óvulo fecundado. En lugar de utilizar óvulos fecundados con donantes humanos, pensamos: ¿Por qué no crear una reproducción artificial de esas fases tempranas, previas a un embrión? Se trata de fabricar lo que se llama un blastocisto. No usamos ni óvulos ni esperma: usamos células madre pluripotentes, ya sean de origen embrionario o células no sexuales ya adultas que han sido tratadas para devolverlas a un estado primordial. Lo interesante de estas células es que tienen la capacidad de convertirse en lo que quieras.
Parece un proceso complejo. ¿Os encontráis con muchas dificultades?
Hay mucha prueba y error, porque si quieres recrear el útero en un chip primero tienes que pensar en cada parte del útero, ya que hay distintas capas y en cada una de ellas el tipo de célula es diferente y necesita su propio ecosistema. Y luego quizás necesitas algún tipo de estimulación mecánica que simule músculos, por ejemplo. Todo esto incrementa la complejidad y significa ir corrigiendo de manera continua muchas pequeñas cosas.
Al tratarse de temas relacionados con la vida, debe tener implicaciones éticas importantes. ¿Es así?
Japón es un país muy riguroso con la ética científica y dependiendo del tipo de células con el que experimentes debes pasar unos protocolos muy estrictos. Para utilizar células de origen embrionario, aunque son de etapas muy anteriores al embrión, tienes que realizar formaciones obligatorias y grabar las sesiones de trabajo, y presentarlas anualmente en la universidad. Las células pluripotentes son más fáciles de manejar en el ámbito ético porque son células que provienen de una persona adulta.
¿Podríais crear vida artificial?
Si por crear «vida» te refieres a «un humano vivo», por ahora no es posible técnicamente. Al estar desarrollando un blastocisto artificial podría pensarse que en potencia se convertiría en un bebé, pero no es viable porque se trata de un cultivo en un tubo, que no puede desarrollarse y convertirse en una vida. Además, hay un comité internacional que establece normas muy estrictas a la hora de manipular células pluripotentes para la creación de modelos embrionarios humanos: estamos obligados a detener el cultivo antes de que aparezcan ciertos marcadores moleculares. Por otro lado, cultivar in vitro cualquier tipo de embrión no es nada trivial y que estos lleguen a desarrollarse fuera de un vientre materno es muy complicado. Hay un equipo en Israel que ha sido capaz de hacer crecer un embrión (natural) de ratón en una especie de vientre artificial, pero por ahora no es posible recrear todo el proceso in vitro.
Para acabar, hay un aspecto curioso de tu trayectoria. Fuiste dobladora de películas y se te puede oír como la niña de Monstruos, S.A. ¿Has pensado en continuar con esa carrera?
Sí, empecé a los tres años porque mi hermano mayor ya trabajaba en ese mundillo. Hace 25 años era un sector muy pequeño que básicamente funcionaba por contactos y, en mi caso, yo hice una prueba porque me lo propusieron un día que lo acompañaba. Estuve trabajando de actriz de doblaje hasta los 18 años. Me gustaba mucho, pero es un mundo que requiere mucha dedicación y disponibilidad. Sería bonito mantenerlo como actividad paralela, pero estando en Japón es difícil. Bueno, ¡y mi talento tampoco es estratosférico!