
Estás leyendo:

Estás leyendo:

22.04.25
10 minutos de lecturaRegenerar la piel o transportar medicamentos a zonas concretas de nuestro organismo es posible hoy gracias a la inspiración que los científicos encuentran en la naturaleza. Tres proyectos apoyados por las convocatorias CaixaResearch de Investigación e Innovación en Salud estudian si animales como los mejillones, los peces cebra o las abejas tienen algunas de las claves para tratar enfermedades que suponen un reto para la comunidad médica internacional.
La naturaleza, a través de miles de millones de años de evolución, ha generado soluciones que permiten a los seres vivos adaptarse a su entorno y sobrevivir. ¿Podemos los seres humanos aprender de quienes ya tienen experiencia demostrada en crear soluciones innovadoras y eficientes? Eso precisamente es lo que hace la biomímesis, una disciplina que se centra en la mejora de la vida humana mediante el estudio y la recreación de estructuras biológicas y sus funciones.
Y es que muchas de las respuestas a los problemas que tenemos hoy podrían encontrarse echando un vistazo a la naturaleza, como ya lo hicieron Leonardo da Vinci, que se inspiró en los pájaros para diseñar máquinas voladoras, o Alexander Fleming, cuyo hallazgo de la penicilina surgió al notar cómo un hongo inhibía el crecimiento de bacterias, lo que dio origen a los antibióticos y revolucionó la medicina.

En el área biomédica, la biomímesis ha generado gran impacto en los últimos años alcanzando importantes logros para la salud humana. Los científicos han conseguido desarrollar materiales biocompatibles, grandes avances en medicina regenerativa e incluso que ciertos medicamentos lleguen a zonas concretas del organismo para aplicar un tratamiento.
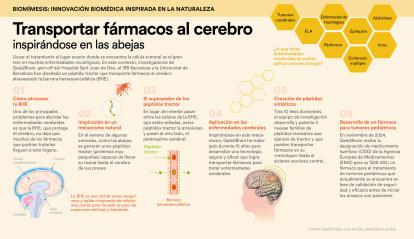
Hacer que el tratamiento llegue al lugar exacto donde se encuentra la célula tumoral es el gran reto en muchas enfermedades oncológicas. A este respecto, investigadores de Gate2Brain, spin-off del Hospital Sant Joan de Déu, el IRB Barcelona y la Universidad de Barcelona, han diseñado un péptido tractor que transporta fármacos al cerebro y atraviesa la barrera hematoencefálica (BHE). Esta tecnología permitirá mejorar el tratamiento de las enfermedades del cerebro, entre ellas el cáncer cerebral infantil, al optimizar la llegada de fármacos a este órgano.
Si bien hasta ahora varios fármacos habían demostrado una actividad antitumoral potente, todos habían fracasado en ensayos clínicos porque no podían atravesar la BHE para llegar al tumor. «Es una barrera protectora celular que solo permite que determinadas moléculas de la sangre circulante entren en el sistema nervioso central para evitar la entrada de patógenos y otras sustancias nocivas», apunta la doctora Meritxell Teixidó, CEO y cofundadora de Gate2Brain, que cuenta con la colaboración de la Unidad de Investigación en Cáncer Infantil - Fundación ”la Caixa” del Hospital Sant Joan de Déu.

El equipo de trabajo liderado por Teixidó —que recibió la ayuda de RecerCaixa, CaixaImpulse Validate y CaixaImpulse Consolidate— estudió el potencial de los péptidos encontrados en los venenos de los escorpiones y las abejas para funcionar como tractores moleculares. «Buscábamos péptidos, que son proteínas muy pequeñas, que actuaran como tractores moleculares para transportar el fármaco hasta el cerebro; y comprobamos que la abeja, así como muchos otros animales, genera en su veneno un péptido tractor que lleva su toxina hasta el sistema nervioso central, pero que podría también llevar fármacos para curar», explica. «Estos tractores no es que pasen entre las células de la BHE, que están selladas, sino que entran en ellas y salen al otro lado, al parénquima cerebral», puntualiza.
En general, mejorar la llegada del fármaco al cerebro supone significativos beneficios para el paciente, pues la aplicación de la dosis exacta mejora la efectividad del tratamiento y reduce los efectos secundarios.

Además, los resultados obtenidos tienen el potencial de aplicarse a otros agentes terapéuticos y barreras biológicas, con implicaciones clínicas significativas. «Hay muchos candidatos a fármacos en enfermedades del cerebro, pero el 98 % necesitarán algún tipo de tractor. Nuestra tecnología podría aplicarse en muchas de ellas», certifica la investigadora.
En noviembre de 2024, Gate2Brain alcanzó un hito decisivo en la lucha contra los tumores cerebrales pediátricos al recibir la Designación de Medicamento Huérfano (Orphan Drug Designation, ODD) de la Agencia Europea de Medicamentos (EMA) para su innovador producto, G2B-002. Actualmente, el proyecto se encuentra en fase preclínica regulatoria en un punto de salto de pruebas entre los roedores y los no roedores (cerdos, en concreto). «Aunque el ensayo clínico está previsto para dentro de tres años, estamos en un momento muy relevante para esta tecnología y primer producto», añade la doctora Teixidó.
Su equipo trabaja sin descanso para abrir una nueva era de opciones terapéuticas en un área de alta necesidad no cubierta. «En los últimos años se ha avanzado mucho en el diagnóstico de tumores cerebrales, en terapias más avanzadas, pero sobre todo en el conocimiento de esos tumores para poder hacer una medicina mucho más personalizada; y los tractores pueden ser el ingrediente que ayude a esas terapias a llegar mejor», concluye.
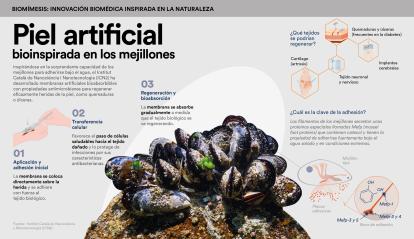
La creación de piel artificial es una necesidad médica de primer orden. El proceso de cicatrización de heridas de la piel, como quemaduras o úlceras (muy frecuentes en enfermedades como la diabetes) es lento y complejo, y desafortunadamente en muchas ocasiones se ve lastrado e incluso bloqueado por la falta de tratamientos efectivos.
El equipo de Salvio Suárez, investigador del Institut Català de Nanociència i Nanotecnologia (ICN2), ha desarrollado una familia de membranas artificiales, bioinspiradas en la capacidad de los mejillones de adherirse bajo el agua, que ya se han validado en estudios preclínicos previos para la regeneración de cartílago y de piel. Los nuevos materiales se adhieren al tejido biológico, son bioabsorbibles, tienen propiedades antimicrobianas y son capaces de transferir células al tejido dañado y promover así su regeneración.

Tal y como explica Suárez, «primero nos centramos en el cartílago y comprobamos que la regeneración era muy positiva, lo que nos llevó a la regeneración de piel porque nos permitía estudiar la membrana en mayor amplitud». Luego realizaron un segundo estudio preclínico para la regeneración de heridas comunes y vieron que podían reducir hasta la mitad el tiempo necesario para restaurarlas. En la actualidad están inmersos en un segundo ensayo preclínico en cerdos, «ya que las características de la piel de estos animales son más similares a las de la piel humana».

Este proyecto, apoyado por la convocatoria CaixaImpulse de Innovación en Salud, pretende optimizar y validar membranas artificiales que tengan a la vez capacidades regenerativas y antibacterianas. «Las propiedades antimicrobianas se deben a las moléculas de los mejillones en las que nos inspiramos», argumenta el experto en ciencia de materiales. Su ventaja es que poseen la capacidad de oxidarse con el tiempo. «Las membranas que nosotros producimos, al bioinspirarse en esas moléculas, también se van oxidando y generan especies químicas, como el peróxido de hidrógeno [el agua oxigenada], con propiedades desinfectantes». Además, este mecanismo antimicrobiano todavía no ha generado resistencias por parte de las bacterias. «Por lo tanto», asegura Suárez, «tenemos un amplio espectro de actuación, incluso para bacterias multirresistentes».
Esta técnica disruptiva puede disminuir el tiempo de hospitalización, reducir las infecciones, muy frecuentes en pacientes quemados, y en última instancia minimizar también el rechazo del injerto. «Lo que buscamos», apunta el investigador, «es que esa piel nueva se parezca lo máximo posible a la original. Desde un punto de vista funcional hemos conseguido que tenga propiedades de flexibilidad, permeabilidad y sensibilidad similares».
Los investigadores, además, se plantean extender su posible uso al tratamiento de otras enfermedades. «Estamos validando sus propiedades para la regeneración neuronal y también para el tratamiento de cierto tipo de tumores», asegura.
El objetivo final es llevar a cabo un primer ensayo clínico en humanos. «Se espera que podamos comenzar el reclutamiento de pacientes en la segunda mitad de 2026», concluye. Además, los investigadores acaban de constituir la empresa Tirecat Health SL para seguir este desarrollo y el de otras aplicaciones de su tecnología.
De acuerdo con la Organización Mundial de la Salud (OMS), hasta medio millón de personas en todo el mundo sufren cada año una lesión de la médula espinal. Los programas de rehabilitación pueden ayudar a recuperar algunas funciones y reducir el riesgo de complicaciones, pero hasta el momento no existen tratamientos capaces de revertir el daño permanente.
Recientemente, un proyecto respaldado por la convocatoria CaixaResearch de Investigación en Salud en colaboración con la Fundação para a Ciência e a Tecnologia (FCT) ha identificado nuevos posibles tratamientos.

Leonor Saúde, investigadora del Gulbenkian Institute for Molecular Medicine de Lisboa, está especializada en biología del desarrollo y ha estudiado ampliamente los procesos embrionarios del pez cebra. Ella y su equipo repararon en una sorprendente capacidad que tiene este diminuto pez de agua dulce: al cabo de dos o tres semanas de sufrir una lesión medular espinal vuelve a nadar con normalidad, pues recupera la movilidad y la sensibilidad en la zona. En cambio, mamíferos como los ratones suelen alcanzar muy poca mejoría en este periodo de tiempo. «Vimos una oportunidad de obtener nuevos conocimientos que tal vez un día podrían aplicarse a pacientes con lesiones en la médula espinal», explica.
El equipo de Saúde investigó minuciosamente ambos animales para determinar la causa de estos resultados tan desiguales. Observaron que los peces cebra, como nunca dejan de crecer, nunca dejan de crear neuronas, de modo que, si sufren una lesión en la médula espinal, pueden sustituir las neuronas perdidas por otras nuevas. «Tampoco forman cicatriz alrededor de la lesión ni sufren inflamación crónica», explica la experta.
Sin embargo, la gran sorpresa para el equipo fue «la desigual cantidad de células senescentes en cada uno de los modelos», revela Saúde. «Se trata de unas células que se van acumulando con la edad en cualquier tejido del cuerpo. Así que, en cierto modo, la senescencia es un indicador del envejecimiento. En los peces cebra, estas células desaparecen del tejido 30 días después de sufrir la lesión. En los modelos con ratones, en cambio, se van acumulando en la zona lesionada».
El equipo de esta investigadora decidió utilizar un fármaco senolítico para reducir el número de células envejecidas en ratones con lesiones de médula espinal y descubrió que la recuperación motora y sensitiva mejoraba. «Concluimos que estas células tienen un efecto negativo en las lesiones medulares: empeoran ostensiblemente la recuperación porque secretan moléculas inflamatorias y profibróticas, que contribuyen a la inflamación y la formación de cicatrices», matiza.
«Actualmente, estamos realizando experimentos de secuenciación de ARN de células individuales para caracterizar mejor estas células y su fenotipo secretor [el conjunto de moléculas que secretan] en momentos específicos después de una lesión», añade la experta. Su objetivo es entender qué tipo de células eran antes de convertirse en senescentes, identificar las moléculas que producen y diseñar estrategias más precisas para manipular estos factores y reducir su impacto negativo en los tejidos.
En el futuro, la investigadora augura que, al ser una condición médica muy compleja, el tratamiento de este tipo de lesiones combinará terapias como la neuroprotección, la neuroestimulación, el trasplante de células madre y quizá otras que aún no conocemos.
La colaboración ha demostrado ser desde siempre un motor clave en el avance científico, pero no el único. Como evidencian estas tres investigaciones, la naturaleza también juega un papel fundamental. Y seguirá haciéndolo. De hecho, «hace apenas tres años se descubrió que había un mamífero —el Acomys o ratón espinoso— que, a diferencia de otros, era capaz de regenerar su médula espinal», revela Saúde. «Aún se está investigando el porqué, pero está claro que los científicos debemos seguir mirando hacia la naturaleza para aprender de ella», concluye.
